식약처, 백내장 수술 점안제 사용 환자 42명 곰팡이균 확인
무균시험 통과 실패 3 품목 대상 내달 4일자 행정처분
안과계를 뜨겁게 달궜던 안내염 논란이 종지부를 찍었다. 품질 부적합 점안제를 사용한 환자에서 실제 곰팡이균이 확인됐기 때문이다.
28일 식품의약품안전처와 질병관리청이 유니메드제약의 '유니알주15밀리그람(히알루론산나트륨)' 등 3개 품목에 대해 품질(무균시험)검사 결과 부적합을 확인해 2월 4일자로 허가를 취소한다고 밝혔다.
해당 품목은 ▲유니알주15밀리그람(히알루론산나트륨) ▲히알론디스포주(히알루론산나트륨) ▲유닐론디스포주(히알루론산나트륨)다.
최근 증가한 백내장 수술 후 진균성 안내염 발생 관련 역학조사 결과, 해당 품목과 진균성 안내염 발생과의 연관성을 확인했다고 밝혔다.
약사법 제62조 위반에 따른 행정처분으로 식약처는 지난해 12월 해당 3개 품목에 대해 잠정 제조‧판매 중지 및 전 제품 회수 조치할 것을 명령했으며, 품질검사 부적합에 따라 해당 품목 허가 취소 처분을 위해 청문 등 행정 절차를 진행해 왔다.
질병청은 지난해 9월~11월 사이 발생한 백내장 수술 후 진균성 안내염 사례 146건 중 136건(93.2%)이 해당 품목을 사용한 것으로 확인됐다.
또한 해당 품목에 대한 식약처 품질검사에서 확보한 진균(곰팡이균)과 해당 품목을 사용한 진균성 안내염 환자 42명의 검체를 배양한 결과 모두 진균(곰팡이균)인 Fusarium spp.가 확인됐다.
한편, 안과 개원가에서는 점안주사제 처방을 받은 환자들의 민원에 대해 우려를 제기한 바 있다.
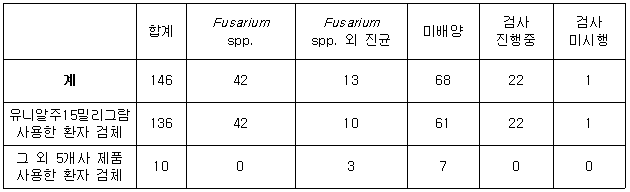
백내장 수술 후 안내염 발생 역학조사 주요 결과
28일 식품의약품안전처와 질병관리청이 유니메드제약의 '유니알주15밀리그람(히알루론산나트륨)' 등 3개 품목에 대해 품질(무균시험)검사 결과 부적합을 확인해 2월 4일자로 허가를 취소한다고 밝혔다.
해당 품목은 ▲유니알주15밀리그람(히알루론산나트륨) ▲히알론디스포주(히알루론산나트륨) ▲유닐론디스포주(히알루론산나트륨)다.
최근 증가한 백내장 수술 후 진균성 안내염 발생 관련 역학조사 결과, 해당 품목과 진균성 안내염 발생과의 연관성을 확인했다고 밝혔다.
약사법 제62조 위반에 따른 행정처분으로 식약처는 지난해 12월 해당 3개 품목에 대해 잠정 제조‧판매 중지 및 전 제품 회수 조치할 것을 명령했으며, 품질검사 부적합에 따라 해당 품목 허가 취소 처분을 위해 청문 등 행정 절차를 진행해 왔다.
질병청은 지난해 9월~11월 사이 발생한 백내장 수술 후 진균성 안내염 사례 146건 중 136건(93.2%)이 해당 품목을 사용한 것으로 확인됐다.
또한 해당 품목에 대한 식약처 품질검사에서 확보한 진균(곰팡이균)과 해당 품목을 사용한 진균성 안내염 환자 42명의 검체를 배양한 결과 모두 진균(곰팡이균)인 Fusarium spp.가 확인됐다.
한편, 안과 개원가에서는 점안주사제 처방을 받은 환자들의 민원에 대해 우려를 제기한 바 있다.








