식약처, 26년간 이상사례 분석…582품목 허가사항 변경
아목시실린, 실로스타졸, 티카그렐러 등 7개 성분(582 품목) 허가사항에 새로운 이상 사례가 추가됐다.
21일 식품의약품안전처는 1989년부터 2015년까지 의약품 사용 후 보고된 이상사례를 분석·평가해 아목시실린 등 7개 성분(582 품목) 허가사항에 새로운 이상사례를 추가하는 안전조치를 실시했다고 밝혔다.
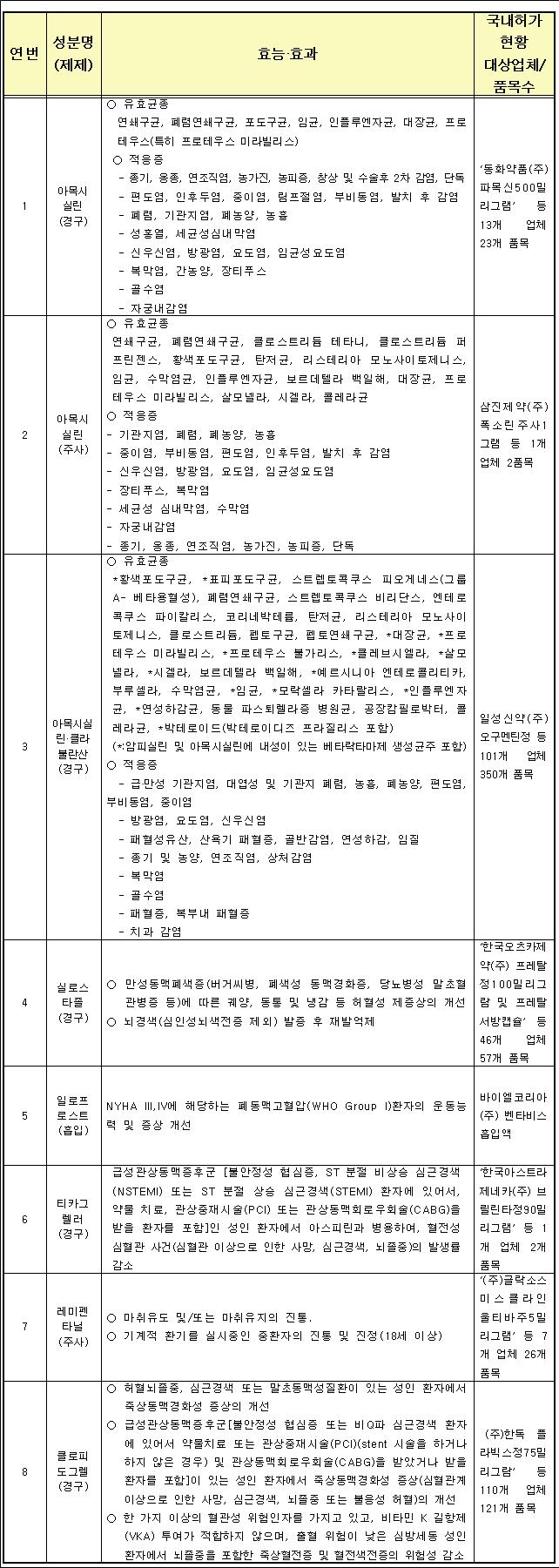
이상사례가 추가된 성분은 ▲아목시실린(경구) ▲아목시실린(주사) ▲아목시실린·클라불란산(경구) ▲실로스타졸(경구) ▲일로프로스트(흡입) ▲티카그렐러(경구) ▲레미펜타닐(주사) ▲클로피도그렐(경구)까지 항생제 2성분, 심혈관계 의약품 4성분, 통증 의약품 1성분이다.
항생제 아목시실린(먹는 약 및 주사 약으로 항생제)은 혈관부종, 반점구진발진 등 발생, 아목시실린과 클라불란산 복합제(먹는 약으로 항생제)는 피부염 등 발생이 추가된다.
심혈관계 의약품인 실로스타졸(먹는 약으로 만성동맥폐색증에 따른 궤양 등의 개선 등에 사용)은 감각저하, 일로프로스트(흡입약으로 폐동맥고혈압 환자의 증상 개선 등에 사용)는 객혈 발생 등이 추가됐다.
또 티카그렐러(먹는 약으로 관상동맥증후군 등에 사용)은 가슴통증, 클로피도그렐(먹는 약으로 동맥경화성 증상의 개선 등에 사용)은 담낭염 등 발생이 추가된다.
통증 의약품인 레미펜타닐(주사 약으로 마취유도 등에 사용)은 혼미 등 발생이 추가된다.
이번 조치는 해당 성분에 대한 이상사례 정보를 한국의약품안전관리원이 약물과 이상사례간의 새로운 잠재적 인과관계 또는 알려진 관계의 새로운 측면을 제시하는 정보를 바탕으로 중앙약사심의위원회의 자문을 거쳐 최종 결정됐다.
21일 식품의약품안전처는 1989년부터 2015년까지 의약품 사용 후 보고된 이상사례를 분석·평가해 아목시실린 등 7개 성분(582 품목) 허가사항에 새로운 이상사례를 추가하는 안전조치를 실시했다고 밝혔다.
이상사례가 추가된 성분은 ▲아목시실린(경구) ▲아목시실린(주사) ▲아목시실린·클라불란산(경구) ▲실로스타졸(경구) ▲일로프로스트(흡입) ▲티카그렐러(경구) ▲레미펜타닐(주사) ▲클로피도그렐(경구)까지 항생제 2성분, 심혈관계 의약품 4성분, 통증 의약품 1성분이다.
항생제 아목시실린(먹는 약 및 주사 약으로 항생제)은 혈관부종, 반점구진발진 등 발생, 아목시실린과 클라불란산 복합제(먹는 약으로 항생제)는 피부염 등 발생이 추가된다.
심혈관계 의약품인 실로스타졸(먹는 약으로 만성동맥폐색증에 따른 궤양 등의 개선 등에 사용)은 감각저하, 일로프로스트(흡입약으로 폐동맥고혈압 환자의 증상 개선 등에 사용)는 객혈 발생 등이 추가됐다.
또 티카그렐러(먹는 약으로 관상동맥증후군 등에 사용)은 가슴통증, 클로피도그렐(먹는 약으로 동맥경화성 증상의 개선 등에 사용)은 담낭염 등 발생이 추가된다.
통증 의약품인 레미펜타닐(주사 약으로 마취유도 등에 사용)은 혼미 등 발생이 추가된다.
이번 조치는 해당 성분에 대한 이상사례 정보를 한국의약품안전관리원이 약물과 이상사례간의 새로운 잠재적 인과관계 또는 알려진 관계의 새로운 측면을 제시하는 정보를 바탕으로 중앙약사심의위원회의 자문을 거쳐 최종 결정됐다.









