숨빗AI, 생성형 의료 AI 'AIRead-CXR' 3등급 인허가
서울대병원 임상으로 유효성 확인…환각 비율 0.3%에 그쳐
[메디칼타임즈=김승직 기자] 의료 인공지능 기업 숨빗AI(대표 배웅)가 국내 최초로 생성형 의료 AI에 대한 식품의약안전처 인허가를 받아내 업계 관심이 쏠린다.
2일 숨빗AI는 자사의 흉부X선 예비소견서(Draft Radiology Report) 생성 솔루션 'AIRead-CXR'(에어리드-씨엑스알)가 식약처 3등급 인허가를 획득했다고 밝혔다.
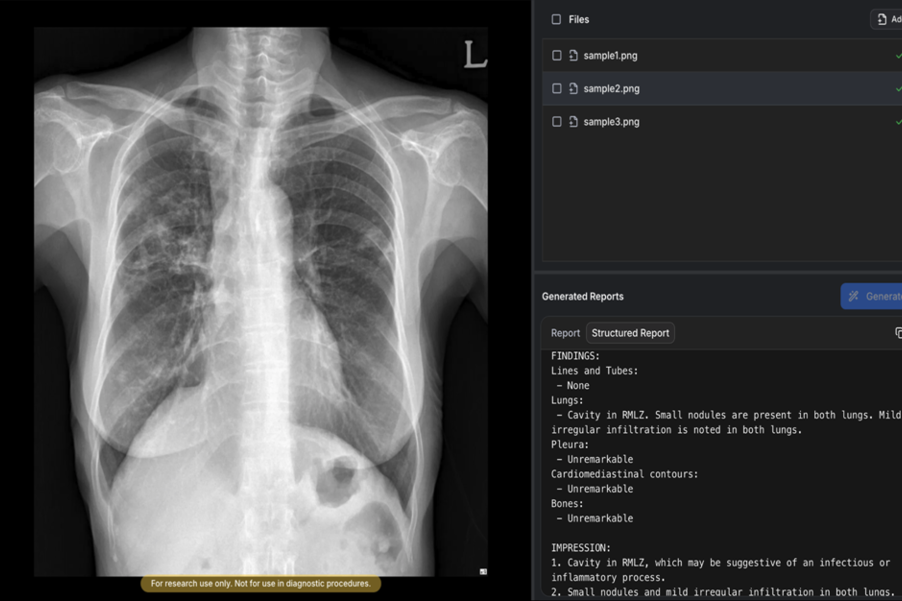
기존 유럽에서 생성형 AI 기반 의료기기가 존재하지만, 의료영상을 직접 분석해 예비소견서를 생성하는 단독 제품으로는 이번 승인이 세계 최초다.
식약처는 전문의 판독문과 AI 초안 간 비교 평가를 통해 유효성과 안전성을 확인했다. 임상은 서울대병원과 분당서울대병원에서 1000 건 이상의 흉부 X선 데이터를 기반으로 확증 단계까지 진행됐다.
AIRead-CXR은 국내외에서 확보한 약 1400만건의 데이터를 학습해, 다양한 병원 환경에서 촬영된 PA 또는 AP 흉부X선에 대해 안정적으로 예비소견서를 제공한다.
핵심적으로 검증된 57개 소견 및 질환에 대해 높은 수준의 판독보조 성능을 제공할 뿐 아니라 이 외의 다양한 영상 소견도 해석·언급할 수 있다. 실제 임상 현장의 워크플로우를 반영해 의료진이 보다 효율적으로 판독 업무를 수행할 수 있도록 설계됐다.
품질 경쟁력도 주목된다. 공개된 임상 논문에 따르면, 흉부영상 전문의들이 평가한 AI 예비소견서 평균 수용도는 85%로, 비교 대상인 MedGemma(66.9%)를 상회했다.
생성형 AI의 대표적 한계인 환각(hallucination) 비율 역시 0.3%로, MedGemma(9.7%) 대비 우수한 안정성을 보였다. 이런 기술력과 임상적 유효성은 영상의학 분야 최고 권위 학술지인 Radiology에 3편, AJR에 1편 이상의 논문으로 뒷받침되고 있다는 게 사측 설명이다.
숨빗AI는 제품 완성도를 높이기 위해 지난 2년간 글로벌 웹데모 'AIRead-CXR'를 전문의 대상으로 운영하며 사용자 피드백을 지속적으로 반영해 왔다. 이런 현장 중심 개선 노력이 이번 인허가와 제품 경쟁력 확보에 중요한 밑거름이 됐다는 평가다.
숨빗AI 배웅 대표는 "세계 최초로 의료영상 분야의 생성형 AI 기반 SaMD 승인을 받게 돼 영광스럽고 감사하다. 많은 분의 도움 덕분에 가능했던 성과"라며 "AIRead-CXR이 흉부X선으로 인한 병·의원 및 영상의학과 전문의들의 업무 부담을 덜어드리고, 더 건강한 세상을 만드는 데 기여하는 제품으로 자리매김하길 기대한다"고 말했다.
이어 "숨빗AI는 first-in-class를 넘어, 고객이 사랑하는 global best-in-class 제품이 되기 위해 더욱 노력하겠다"고 덧붙였다.








