복지부, 모사프리드 등 7개 성분 공개…대웅제약 행보 '주목'
의학적 권고‧임상효용성 평가 구체화…제약사 대응에 맞대응
보건복지부가 발표를 미뤄왔던 '2024년 급여재평가' 대상이 되는 7개 성분 의약품을 공개했다.
한 해 처방 규모만 총 4000억원에 달하는 7개 성분의 기등재 의약품이 사실상 퇴출 위기에 놓이면서 향후 해당 품목을 보유한 제약사들의 대응 여부에 관심이 집중되고 있다.
여기에 정부는 급여재평가 과정에서 가장 큰 잣대가 되는 '임상적 유용성' 항목을 구체화하기로 했다. 치료제 임상근거가 게재된 논문이 있을 시 해당 논문의 질적 수준까지 보겠다는 뜻이다.
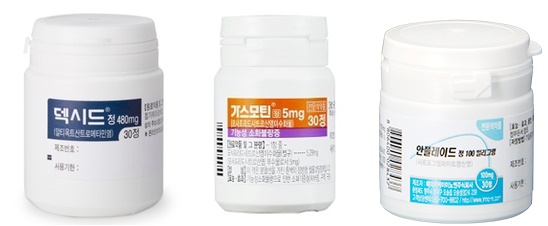
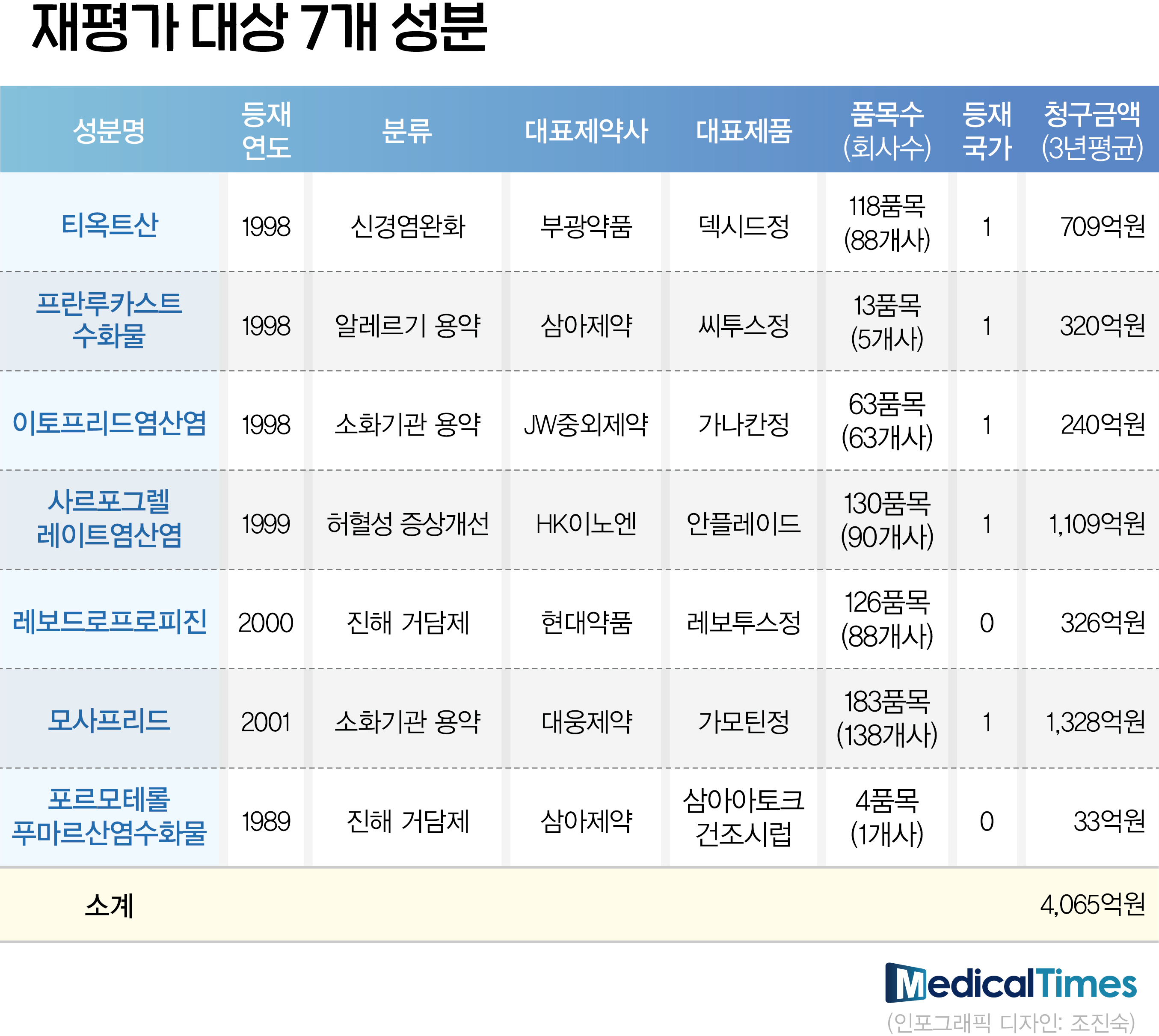
급여재평가 '단골손님'된 내과 다처방 약물
지난 30일 복지부는 건강보험정책심의위원회를 열고 내년도 급여재평가 대상 약제 등을 포함한 '약제 급여 적정성 재평가 추진 계획'을 보고했다.
복지부는 내년에 진행할 급여재평가에는 최종 7개 성분은 ▲티옥트산(thioctic acid) ▲프란루카스트수화물(pranlukast hydrate) ▲이토프리드염산염(itopride hydrochloride) ▲사르포그렐레이트염산염(sarpogrelate hydrochloride) ▲레보드로프로피진(levodropropiaine) ▲모사프리드(mosapride) ▲포르모테롤 푸마르산염수화물(formoterol fumarate hydrate) 등이다.
여기서 가장 관심을 모은 것은 소화기 약물로 내과 병‧의원 다처방 성분인 모사프리드 시장이다.
대웅제약 가스모틴정이 대표품목인 모사프리드 시장의 경우 3년 평균 한해 1328억원에 육박하는 대형 시장이다.
유비스트에 따르면, 대웅제약 가스모틴의 지난해 처방액은 175억원이다. 여기에 가스모틴SR 처방액 91억원을 합하면 한 해 300억원의 매출을 거두는 대형 처방시장.
하지만 내년도 급여재평가 대상으로 퇴출 대상으로 몰리면서 대웅제약을 필두로 제약업계는 임상적 효능을 입증해야 하는 숙제를 떠안게 됐다.
제약업계애서는 가스모틴을 필두로 한 모사프리드 성분이 급여재평가 대상으로 몰리면서 PPI(Proton Pump Inhibitor, 프로톤펌프억제제)와 H2 수용체 길항제(H2RA) 계열 약물이 수혜를 받을 수 있다고 예상했다.
익명을 요구한 A국내사 임원은 "내년도 급여재평가 결과가 나와야 알겠지만 급여에서 퇴출될 경우 PPI나 H2RA 계열 약물이 수혜를 볼 수밖에 없다"며 "내과 중심 시장에서 대체 품목으로 꼽히기 때문이다. 급여재평가도 벌써 3년차에 접어든 시점에서 해당 품목을 보유한 제약사들이 공동전선을 구축할지 여부도 관건"이라고 전했다.
여기에 3년 평균 한 해 1109억원으로 평가된 '사르포그렐레이트' 시장도 내년 급여재평가 대상에 포함되 주목된다.
사르포그렐레이트는 선택적 세로토닌(5-HT2A) 수용체 길항제로 혈소판과 혈관에 작용해 혈관 폐색을 억제하여 만성 동맥폐쇄증에 의한 궤양, 통증 및 냉감 등의 허혈성 증상 개선 효과를 나타낸다. 또한 가역적으로 혈소판 응집을 억제하여 수술 전 휴약기가 약 1일 정도로 짧은 편으로 알려져 있다.
해당 시장의 경우 HK이노엔 안플레이드와 대웅제약 안플원가 후발의약품임에도 시장을 주도하고 있다. 유비스트에 따르면, 지난해 각각 230억원, 217억원의 처방 매출을 거둬 시장을 이끌고 있다.
내과계를 중심으로 한 임상현장에서는 다처방 약물이 급여재평가에 포함되자 대체 향후 대체처방 여부 등을 고민해봐야 한다고 전했다.
대한내과의사회 곽경근 총무부회장(서울내과)은 "의사회 자체적으로 임상현장의 영향을 평가해봐야 한다"며 "아직 공개된 지 초기이기 때문에 내용부터 공유한 뒤 대체 처방 품목도 평가해봐야 할 것 같다"고 전했다.
급여재평가 핵심 '임상적 유용성' 구체화
이 가운데 복지부는 내년도 급여재평가 성분을 공개하면서 평가 잣대가 되는 의학적 권고 및 임상적 유용성 등 항목을 개선하기로 했다.
임상효과성 평가 시 효과를 인정한 문헌의 비율 외에도 문헌의 질적 수준을 종합적으로 고려하겠다는 것이다. 의학적 권고를 인정한 문헌 개수가 다수가 아니더라도 자료의 질적 수준이 높고, 추천정도가 높다면 임상효과가 충분하다고 평가할 수 있다는 것이다.
반대로 임상근거를 인정한 문헌의 질적 수준이 낮다면 이를 인정하지 않을 수 있음을 뜻한다.
이와 관련해 지난 2020년부터 시행한 급여재평가 과정에서 평가 대상으로 올랐던 한림제약 엔테론 등 주요 품목은 평가과정에서 임상근거가 되는 논문 등을 제시하며 급여를 유지해온 바 있다.
결과적으로 의학적 권고의 경우 '교과서, 임상진료지침, HTA 보고서에서 의학적 사용 권고 여부'가 쟁점이 되는 한편, 임상 효과성은 '일정수준 이상(SCIE등재 RCT)의 임상연구문헌에서 임상효과성 여부'가 주요 평가 잣대로 활용될 것으로 보인다.
제약업계에서는 이를 두고 정부가 2020년부터 급여재평가를 진행해오며 제약사가 대응해왔던 방식에 맞대응한 것으로 평가했다.
임상논문도 질적 수준이 높아야 인정해줄 수 있음을 뜻한다는 것이다.
익명을 요구한 제약업계 관계자는 "급여재평가를 시행하면서 퇴출 후보로 몰렸던 일부 품목의 경우 임상적 유용성을 증명하면서 급여를 유지한 사례가 존재했다"며 "급여재평가 전에 임상적 논문 게재를 추진하는 경우도 존재했다. 이 같은 제약업계의 움직임에 정부가 대응한 것"이라고 평가했다.
그는 "임상적 논문을 제시하면서 급여 명맥을 이어가는 것이 제약사의 대응이었는데, 이를 보다 체계적이고 까다롭게 보겠다는 것"이라며 "기존의 제약사의 대응방식도 변화가 불가피하다"고 전했다.








