마운자로 욕심 과했나 끝내 약가 합의 실패…'약가유연' 모델 불발
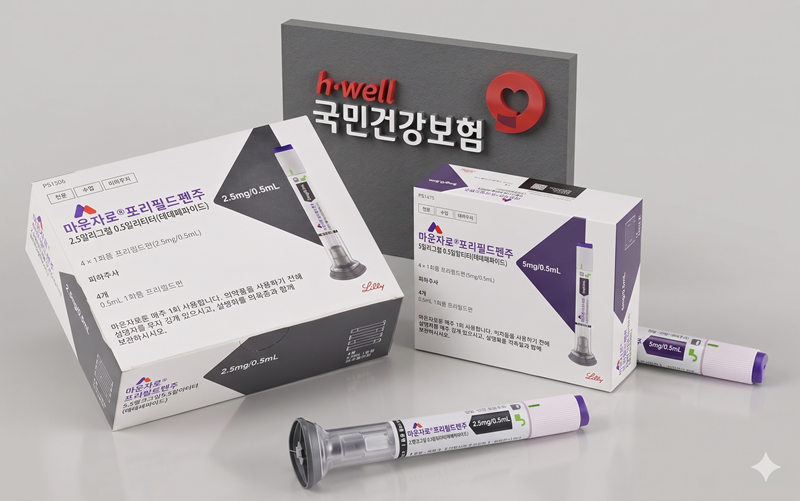
[메디칼타임즈=문성호 기자]한국릴리의 당뇨·비만 치료제 '마운자로(터제파타이드)'의 급여 등재가 최종 결렬됐다. 정부가 혁신 신약의 가치를 인정해 도입한 '약가유연계약제'의 적용 모델로 기대를 모았지만, 끝내 제약사와 보험당국 간의 간극을 좁히지 못한 것으로 확인됐다.한국릴리 당뇨병 및 비만 치료제 마운자로 프리필드펜주 제품사진.13일 제약업계에 따르면, 국민건강보험공단과 한국릴리는 마운자로의 당뇨병 적응증 신규 등재를 위한 약가 협상을 한 차례 연장하며 진행했으나 최종 합의에 도달하지 못하고 협상이 종료됐다.이번 협상의 최대 쟁점은 표시가격은 글로벌 수준으로 유지하되 실제 가격과의 차액을 제약사가 환급하는 '약가유연계약제'의 적용 여부였다. 정부가 해당 제도 도입을 본격화함에 따라 업계에서는 마운자로가 '1호 대상 약제'가 될 것으로 내다봤다. 릴리 역시 글로벌 약가 체인을 방어하기 위해 해당 제도를 바탕으로 협상에 임했으나, 보험당국과 '약가' 합의점을 도출하는 데 실패했다.특히 이번 협상 결렬과 맞물려 앞서 등재된 경쟁 약물인 노보노디스크제약 '오젬픽(세마글루타이드)'의 약가도 새삼 주목받고 있다. 오젬픽은 올해 상반기 급여 등재 당시 기존 GLP-1 유사체인 '트루리시티(둘라글루타이드)'의 낮은 약가 수준을 수용하며 시장에 진입한 바 있다.실제로 건강보험심사평가원 고시에 따르면, 오젬픽(2mg/1.5mL 용량 기준) 한 펜의 보험 상한가는 7만 3528원이다. 이를 주 0.5mg 투여 기준인 4주 치로 나누면 주당 소요 비용은 약 1만 8382원 수준이다. 이는 대체약제인 트루리시티 최저 용량(0.75mg)의 상한가인 1만 8376원과 사실상 일치한다. 결국 보험당국이 차세대 혁신 신약의 가치를 이전 세대 약제의 '최저 용량' 가격에 묶어버린 셈이며, 이것이 마운자로 협상의 보이지 않는 '가이드라인'으로 작용했다는 의견이 나오고 있다.결과적으로 GIP/GLP-1 이중 작용제로서 차별화된 임상적 가치와 글로벌 약가 유지를 주장한 릴리와, 기존 약제와의 형평성 및 재정 건전성을 강조한 정부의 입장 차이는 협상 연장 기간 동안에도 좁혀지지 않은 셈이다.마운자로의 급여 진입이 무산됨에 따라 임상 현장의 혼란도 불가피할 전망이다.당뇨병 치료의 새로운 패러다임을 기대했던 의료진과 환자들은 마운자로를 해당 적응증으로 처방받기 위해서는 당분간 높은 비급여 비용을 감수해야 할 처지에 놓였다. 다만, 릴리 측은 약가협상 실패를 인정하면서도 재도전 의지를 분명히 했다. 릴리 관계자는 "마운자로의 보험 등재를 위해 최대한 신속히 재신청할 수 있는 방안을 모색할 예정"이라며 "더 많은 국내 당뇨병 환자들에게 치료 옵션을 제공하기 위해 정부와 긴밀히 협력해 나가겠다"고 밝혔다.